 对照组。 结果 治疗2个月后,观察组完全缓解0例,部分缓解17例,稳定11例,进展0例,临床获益率为100.00%,临床有效率为60.71%。对照组完全缓解0例,部分缓解9例,稳定15例,进展6例,临床获益率为80.00%,临床有效率为33.33%。观察组临床获益率与临床有效率明显高于对照组(P<0.05)。观察组皮疹12例(42.8%),腹泻7例(25.0%),乏力24例(85.7%),脱发6例(21.4%),粒细胞降低2例(7.1%)。对照组皮疹11例(36.7%),腹泻7例(23.3%),乏力25例(83.3%),脱发7例(23.3%),粒细胞降低4例(13.3%)。两组不良反应比较差异无统计学意义(P>0.05)。 结论 厄洛替尼辅助全脑放疗治疗非小细胞肺癌脑转移患者具有较好的临床疗效,值得推广应用。
对照组。 结果 治疗2个月后,观察组完全缓解0例,部分缓解17例,稳定11例,进展0例,临床获益率为100.00%,临床有效率为60.71%。对照组完全缓解0例,部分缓解9例,稳定15例,进展6例,临床获益率为80.00%,临床有效率为33.33%。观察组临床获益率与临床有效率明显高于对照组(P<0.05)。观察组皮疹12例(42.8%),腹泻7例(25.0%),乏力24例(85.7%),脱发6例(21.4%),粒细胞降低2例(7.1%)。对照组皮疹11例(36.7%),腹泻7例(23.3%),乏力25例(83.3%),脱发7例(23.3%),粒细胞降低4例(13.3%)。两组不良反应比较差异无统计学意义(P>0.05)。 结论 厄洛替尼辅助全脑放疗治疗非小细胞肺癌脑转移患者具有较好的临床疗效,值得推广应用。
[关键词] 厄洛替尼;非小细胞肺癌;放疗;脑转移
[中图分类号] R739.4 [文献标识码] B [文章编号] 1673-9701(2015)28-0037-04
肺癌脑转移是肺癌晚期常见并发症之一,随着肺癌发病率的逐年升高,针对肺癌脑转移的防治也愈加受到重视[1]。目前临床常用的肺癌脑转移的治疗方法为全脑放疗,随着治疗方式的逐渐应用及完善,研究表明,治疗期间加入小分子药物联合治疗可提高放疗效果的作用[2]。厄洛替尼是一种酪氨酸激酶选择性抑制剂,临床中已经将其应用于表皮生长因子受体基因(epidermal growth factor receptor,EGFR)突变的非小细胞肺癌晚期的一线或二线治疗中,有研究表明[3],将其应用于放疗过程中可提高放疗治疗有效率。本研究中,选取2010年1月~2014年12月来我院治疗的非小细胞肺癌脑转移患者共计28例,探讨厄洛替尼辅助全脑放疗治疗非小细胞肺癌脑转移患者的临床疗效,现报道如下。
1 资料与方法
1.1 一般资料
选取2010年1月~2014年12月期间来我院采取治疗的非小细胞肺癌脑转移患者共计28例为观察组,结合家庭条件及患者意愿,所有患者均自愿选择厄洛替尼辅助全脑放疗进行治疗。男18例,女10例。年龄42~75岁,平均(61.9±4.5)岁。所有患者经病理学或细胞学检查全部符合肺癌的诊断标准,确诊为非小细胞肺癌,且经影像学检查证实存在肺癌脑转移[4]。28例患者中,14例肺腺癌,6例肺腺鳞癌,8例肺鳞癌。纳入标准[5]:①确诊为非小细胞肺癌,存在脑转移;②化疗失败患者或对化疗不耐受患者;③脑转移病灶2个或2个以上。排除标准:①放疗禁忌证者;②厄洛替尼药物禁忌证者;③预计生存期短于4周;④合并其他系统严重疾病。本次研究经伦理委员会批准,所有患者均签署知情同意书。选取同期非小细胞肺癌脑转移30例为对照组,该组人群均选择单纯性放疗,未接受药物治疗。男19例,女11例,平均年龄(61.9±4.6)岁。两组患者在性别、年龄、病情方面比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
所有患者均给予常规内科对症和支持治疗,如缓解颅内水肿等。在此基础上进行全脑放疗治疗以及厄洛替尼(上海罗氏制药有限公司,150 mg×7粒,国药准字J20120060)辅助治疗。患者采取仰卧位,定位以及照射均使用热塑面膜固定头部,以保证治疗的重复性。CT模拟定位,使用6-MVx线三维适形放疗技术,照射剂量,3 Gy/次,总剂量DT=30 Gy/10 Fx。放疗频率5次/周,放疗同时口服厄洛替尼150 mg/d,1次/d,服用药物30 d以上或至病灶进展以及患者不耐受[6]。对照组则仅给予全脑放疗治疗,方法同观察组。观察2个月后的临床治疗效果。
1.3 评价标准
根据实体瘤疗效评定标准(response evaluation criteria in solid tumors,RECIST)[7]进行评定,完全缓解:病灶消失,肿瘤标志物水平正常;部分缓解:基线病灶长径缩小在30%及以上;稳定:基线病灶长径缩小在30%以下或未增加至20%;进展:基线病灶长径增加20%以上或发现新发病灶。
临床获益率=(完全缓解例数+部分缓解例数+稳定例数)/总例数×100%。临床有效率=(完全缓解例数+部分缓解例数)/总例数×100%。
1.4 观察指标
观察两组患者临床治疗效果,对比不良反应发生情况。
1.5 统计学方法
采用SPSS19.0统计学软件分析,计数资料比较采取χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组临床治疗效果比较
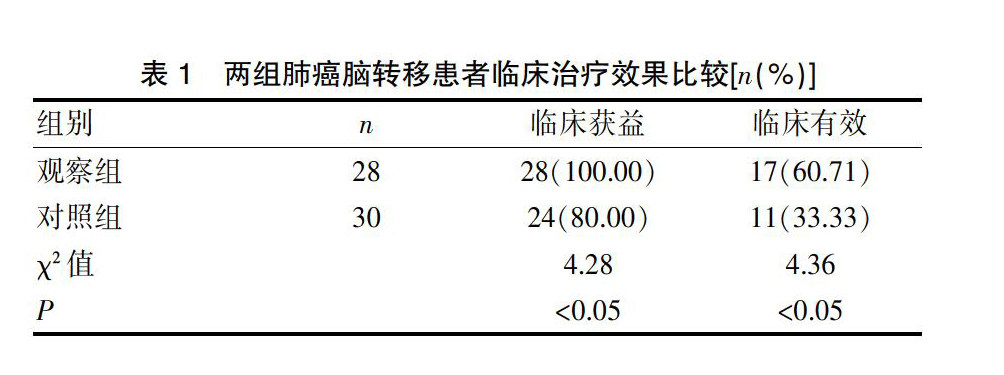
治疗2个月后观察组完全缓解0例,部分缓解17例,稳定11例,进展0例,临床获益率为100.00%,临床有效率为60.71%。对照组完全缓解0例,部分缓解9例,稳定15例,进展6例,临床获益率为80.00%,临床有效率为33.33%。观察组临床获益率与临床有效率明显高于对照组(P<0.05)。见表1。
表1 两组肺癌脑转移患者临床治疗效果比较[n(%)]
2.2 不良反应
观察组发现皮疹12例(42.8%),腹泻7例(25.0%),乏力24例(85.7%),脱发6例(21.4%),粒细胞降低2例(7.1%)。对照组发现皮疹11例(36.7%),腹泻7例(23.3%),乏力25例(83.3%),脱发7例(23.3%),粒细胞降低4例(13.3%)。两组不良反应比较差异无统计学意义(P>0.05)。见表2。
3 讨论
肺癌脑转移是肺癌晚期常见的并发症之一,有分析显示,从理论上分析,由于血脑屏障的存在,肺癌细胞并不容易进入脑组织中从而形成脑部转移灶。但因为椎动脉及椎动脉丛及内部血管存在较多吻合支,为肺癌细胞的脑部转移提供一定的生理结构基础,使之可以通过心脏泵血至颈动脉从而上至脑组织处形成转移[8]。一旦形成肺癌脑转移后,患者后期可表现为颅内高压,出现头痛、呕吐症状,或者癌细胞侵袭脑部神经,致使其疼痛难忍同时影响脑部神经正常功能,肢体出现功能障碍,最终危及患者生命[9]。对于肺癌单发或者多发脑转移(多以多发转移为主),全脑放疗是较为有效的姑息方法之一,因肺癌脑转移中病灶多为边界清晰的规则形状,常为圆形,放射适形度较好,且与周围组织边界清晰,有利于放疗技术的实施。因此放射治疗被认为是晚期肺癌脑转移的一种标准治疗手段[10]。也有其他文献曾报道选择手术切除单发脑转移灶,对局部控制有一定的疗效,但具有其他组织转移风险,手术并发症大,患者一般难以接受。其他区别于全脑放疗的立体定向放疗(珈马刀)治疗方式,对单发脑转移灶也有文献报道有一定的临床疗效,甚至有的达到完全缓解。但适应证一般要求病灶直径<3 cm、单发、病灶不能位于重要功能区。对多发脑转移灶不宜行立体定向放疗。所以,目前对于肺癌脑转移的患者进行全脑放疗仍是十分有效、可行的、常规的治疗手段。
近年来,选择小分子酪氨酸激酶抑制剂作为一线或二线治疗EGFR突变的晚期非小细胞肺癌的治疗药物已经逐渐走向常规。厄洛替尼就是小分子酪氨酸激酶抑制剂其中的一种,为分子靶向药物[11],半衰期为36 h,经粪便排出体外。虽然目前厄洛替尼抗肿瘤的作用机制未全部明确,但其可有效抑制酪氨酸激酶的磷酸化,阻止其自体活化,使其参与的信号通路被抑制,同时促进抑制细胞周期的p27的生成,抑制癌细胞的增长[12]。在抑制酪氨酸激酶活化的过程中,厄洛替尼与其的亲和力及选择性比同为小分子药物的吉非替尼更有效。在部分体外及体内试验中表明,厄洛替尼可以提高放疗对肺癌脑转移病灶的杀伤敏感度,联合全脑放疗的效果优于常规放疗。
本研究结果显示,治疗2个月后观察组完全缓解0例,部分缓解17例,稳定11例,进展0例,临床获益率为100.00%,临床有效率为60.71%。观察组临床获益率与临床有效率明显高于对照组(P<0.05),本结果表明应用厄洛替尼确实可增强治疗肺癌脑转移的临床疗效,结果与同领域其他研究基本相符[13]。分析厄洛替尼增强全脑放疗疗效的可能原因如下:首先,厄洛替尼作用敏感期主要集中于G1期[14],相对于放疗中敏感期G2期有所差异,使厄洛替尼辅助全脑放疗时可加强放疗不敏感期的肿瘤细胞抑制,从而提高杀伤肿瘤细胞的有效率。其次,厄洛替尼可降低放疗后对正常组织的损伤。同时,研究表明,厄洛替尼可通过抑制PI3K/AKT通路促进肿瘤细胞凋亡,并且抑制EGFR各通路网络中磷酸化,降低肿瘤细胞继续增殖的可能[15],增强放疗对肿瘤细胞的杀伤效果。
对治疗后观察组出现的不良反应进行统计发现,皮疹及乏力为最常见的不良反应,分别占42.8%和85.7%,其余为腹泻、脱发,还有部分患者出现粒细胞降低现象,分别占25.0%、21.4%及7.1%。该结果与其他研究中结果基本一致[16],不良反应相对较轻,治疗期间患者耐受性相对较好。但是,本研究中因患者数量限制选取样本量相对较少,只对脑转移病变疗效做了初步分析,未对颅外全身病变进一步评价分析。为了得到更为精确、更具有参考价值的数据,将来应选择更大样本量及更多监测指标进一步探索。另外,本研究未对患者进行EGFR突变的检测,EGFR突变状态与颅内病灶疗效相关,突变阳性与阴性患者之间临床差异有多大?本研究因病例数少未做深入分析。有待扩大样本量进一步临床研究。
综上所述,厄洛替尼辅助全脑放疗治疗肺癌脑转移患者具有较好的临床疗效,临床上值得推广使用。
[参考文献]
[1] 王德钦. 姑息疗法治疗的肺癌脑转移患者生存期的影响因素分析[J]. 山东医药,2013,53(1):65-66.
[2] 蒋晓东,丁曼华,乔云,等. 内皮抑素联合放疗治疗肺癌脑转移及其获益人群筛选的临床研究[J]. 中华行为医学与脑科学杂志,2014,23(2):122-125.
[3] 刘勇,赵荆,于世英,等. 厄洛替尼对非小细胞肺癌脑转移放疗后复发/进展的疗效观察[J]. 医药导报,2012,31(1):20-23.
[4] 罗绍友,陈红,房芳,等. 厄洛替尼治疗吉非替尼耐药老年非小细胞肺癌脑转移的疗效[J]. 临床荟萃,2012,27(4):301-303.
[5] 庄洪卿,袁智勇,王军,等. 全脑放疗联合厄洛替尼治疗肺腺癌多发脑转移的理论基础和研究进展[J]. 中华放射肿瘤学杂志,2012,21(6):546-549.
[6] Juhász E,Kim JH,Klingelschmitt G,et al. Effects of erlotinib first-line maintenance therapy versus placebo on the health-related quality of life of patients with metastatic non-small-cell lung cancer[J]. European journal of cancer:official Journal for European Organization for Research and Treatment of Cancer (EORTC) [and] European Association for Cancer Research(EACR),2013,49(6):1205-1215.
[7] Tsuchida Y,Therasse P. Response evaluation criteria in solid tumors (RECIST): New guidelines[J]. Medical and Pediatric Oncology,2001,37(1):1-3.
[8] 江昊,李娈,邓鹏,等. 厄洛替尼单药与替莫唑胺联合放疗对肺腺癌伴脑转移的临床疗效分析[J]. 现代生物医学进展,2014,14(13):2476-2479,2490.
[9] 张洁霞,蔡迪,李时悦,等. 非小细胞肺癌脑转移厄洛替尼和吉非替尼治疗临床比较[J]. 中华肿瘤防治杂志,2015,22(4):285-288.
[10] 朱虹,李云海,王洪林,等. 非小细胞肺癌脑转移厄洛替尼结合全脑放疗治疗的理论基础和研究进展[J]. 国际肿瘤学杂志,2014,41(6):435-438.
[11] 曹梦苒,刘秀峰,华海清,等. 厄洛替尼治疗难治性肺鳞癌合并脑转移1例[J]. 临床肿瘤学杂志,2013,18(4):383-384.
[12] 张栋,牟晓燕,孙尔莲,等. 厄洛替尼一线治疗非小细胞肺癌并脑转移1例[J]. 医学影像学杂志,2014,24(9):1486,1524.
[13] 万欣,王军,吴凤鹏,等. 厄洛替尼治疗晚期非小细胞肺癌临床观察[J]. 中华肿瘤防治杂志,2014,21(19):1538-1543.
[14] 袁岳宏,林连兴. EGFR-TKI联合同步放疗一线治疗EGFR突变型Ⅳ期非小细胞肺癌的临床观察[J]. 广东医学,2012,33(12):1767-1769.
[15] 江再茂,丁江华,左新年,等. 厄洛替尼一线治疗老年非小细胞肺癌脑转移7例疗效观察[J]. 安徽医药,2012,16(6):824-825.
[16] 孙健,刘宁波,庄洪卿,等. 厄洛替尼和塞来昔布联合应用对人肺腺癌A549细胞放射增敏的研究[J]. 中华放射医学与防护杂志,2012,32(2):186-190.
(收稿日期:2015-06-25)